体外诊断类产品作为医疗器械中一个分类,有它的独特性。所以对于他的创新信息进行一个分析,有助于我们了解这个行业的发展。
一、公示件趋势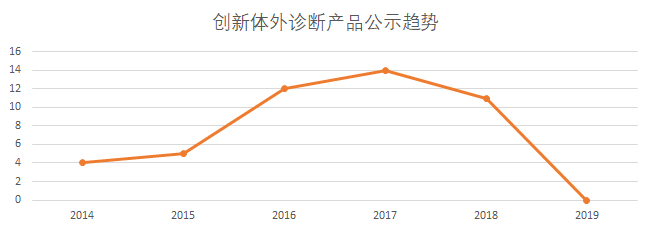
今年无体外诊断类产品的创新公示,是趋势中最大变化。因数据未公布,不知道申请数有多少。
二、申请区域分布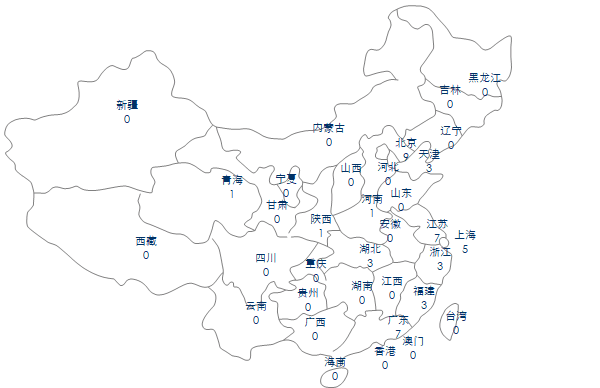
区域(剔除进口的3件)分布上,北京、广东、江苏位居前三,与注册批准情况基本一致(IVD注册情况参考)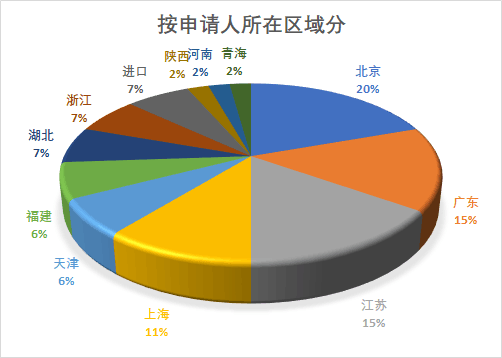
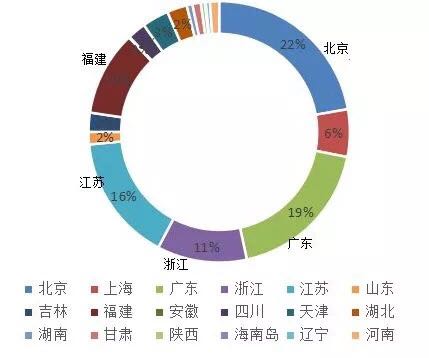
三、按待测物分类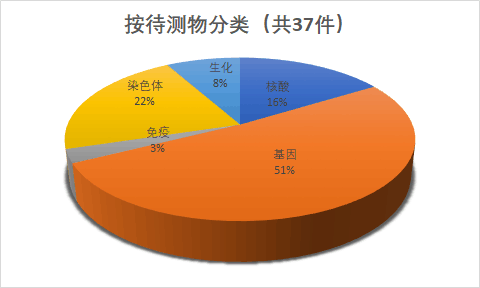
创新的产品待测物主要集中在基因和核酸(剔除仪器类9件)
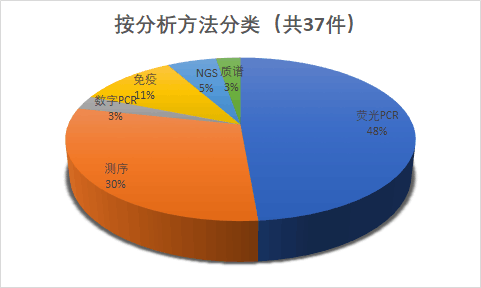
PCR荧光、测序测试方法引领潮流(剔除仪器类9件)
五、其它
在公示的创新体外诊断试剂中,有5件跟EGFR基因相关的检测试剂盒,荧光PCR、数字PCR、测序等各种前沿测试方法轮番上阵,也算创新里面的各特别现象了。
数据来源CMDE
参考:
https://www.qianzhan.com/wenda/detail/190427-969b6ca0.html


Comments | NOTHING