本文数据来源NMPA官网,获批信息为“肺结节CT影像辅助检测软件获批上市”文后的附表,其它数据来自NMPA产品注册数据库。因部分医疗器械需要组合使用,本文统计时这类器械组合体按一个统计。所以公示98个产品,实际上是91个审查公示的产品。统计期为截止到2020年12月11日。
一、按年度分布
统计期内,共295个医疗器械创新产品通过CMDE“创新医疗器械特别审查申请审查结果公示”。
从年度公示数量上来统计,2017年度以52个占据第一位,2014年度以17个垫底。可以肯定的是2020年度将稳据第二位;
从年度获批数量上来说,2016年度和2017年度年以22个领先;
从每年获批比例上来看,2015年度年以68.97%领先,这个跟时间长度有关;
从年度的平均产品获批时长(按公示至获批日期计算,下同)来看,产品获批时长逐年下降,这应与公示产品的成熟程度逐年提供有关系,也从侧面可以看出“创新医疗器械特别审查申请审查”越来越完善。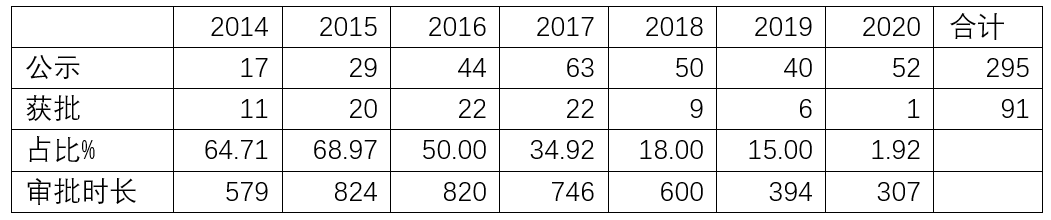
二、按申请区域分布
全国共有18个省、直辖市,共258个产品(不含进口)通过创新器械审查。
北京以23个获批产品领先,获批率37.7%;安徽与福建公示的产品均已全部获批;另外四川、山西、江西、河南、湖南所有公示的产品(共10个)无获批记录;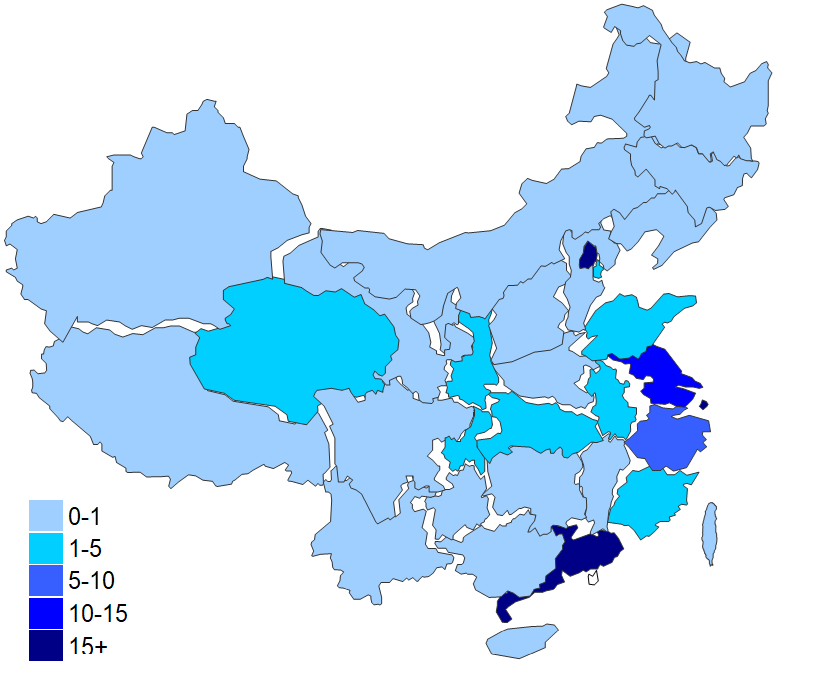
三、审批时长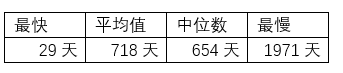
统计期内,产品获批时长平均值718天,中位数654天。
最长是江苏益通生物科技有限公司“周围神经修复移植物”,它于2015年6月26日公示,2020年11月17日获得批准(国械注准20203130898)(该产品目前无法在NMPA注册数据库中查到)。
https://www.cmde.org.cn/CL0050/3690.html
https://www.nmpa.gov.cn/zwfw/sdxx/sdxxylqx/qxpjfb/20201118140611173.html
最快的是海杰亚(北京)医疗器械有限公司的“低温冷冻手术系统(包含一次性使用无菌冷冻消融针)” 2017年1月16日公示,2017年02月14日获得批准(国械注准20173583088/89)。
https://www.cmde.org.cn/CL0050/5975.html
四、按产品类别
统计期间内,获批产品在新的22个产品类别中覆盖了13个;“22 临床试验器械”以22个占第一位,这个跟该类别产品众多有关。
各个产品类别的产品获批时长,“21医用软件”最快,平均290天,“08 呼吸、麻醉和急救器械”最长,这个产品获批时长跟产品特性有较高的吻合度。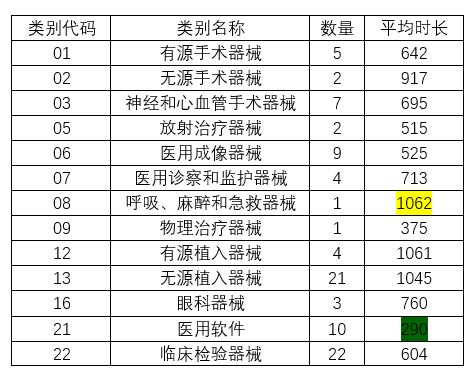
科技驱动发展 创新引领未来 alberf与你一起关注


Comments | NOTHING