本文数据来源NMPA官网发布的产品的批件数据、月度统计数据和月度批准数据,仅供参考。本文仅对2022年首次注册的数据进行分析,特此告示。
前言
2月8日,国家药监局发布了《2022年度医疗器械注册工作报告》,从宏观方面来分析,类目很丰富,数据很详细,但没有IVD方面的数据。这次我续《2022年国产三类医疗器械分析——注册人篇》后的第二篇,尝试对2022年的第三类IVD(6840)做个的统计分析,抛砖引玉,欢迎大家讨论。
备注:我引用的总数据是1843个(参见上篇文章),其中318个IVD,包含68个新冠相关检测试剂。是经过核对的无重复的。正文目录:
★ 注册人获证数;
★ 注册人属地分布(省、市);
★ 方法学分布;
★ 申报时长统计;
注册人分布
151个境内注册人获得318个IVD注册证
★ 注册人获批最大值为22个,与同期医疗器械注册人获批最大值一致;
★ 每个注册人平均值为2.11,略高于同期医疗器械注册人平均值2.00,集中度稍高;
★ 有88个注册人获批1张,29个注册人获批2张,获批8个以上的均只有1家;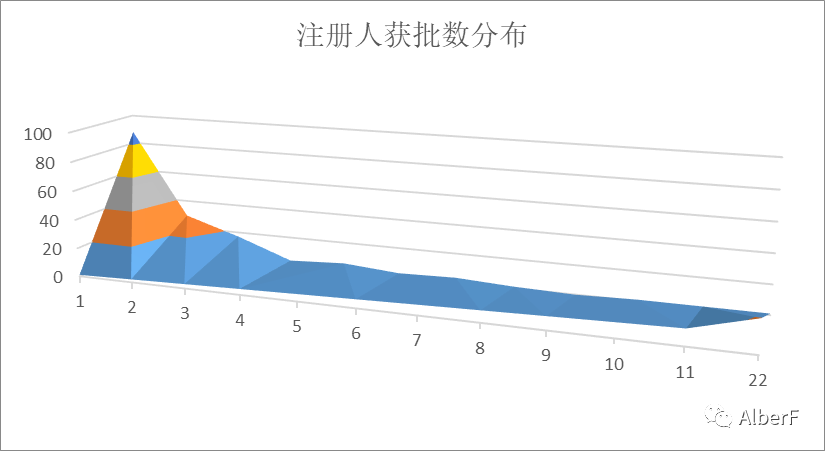
上图X轴为持有注册证数量,Y为持有x的注册人数
省市分布
广东省获证92张,位居第一
★ 17个省市有产品获证,港澳台另计;获证省份中,均值为18.70,中位数11;
★ 获证省份中,均值为18.70,中位数11,分布比较集中;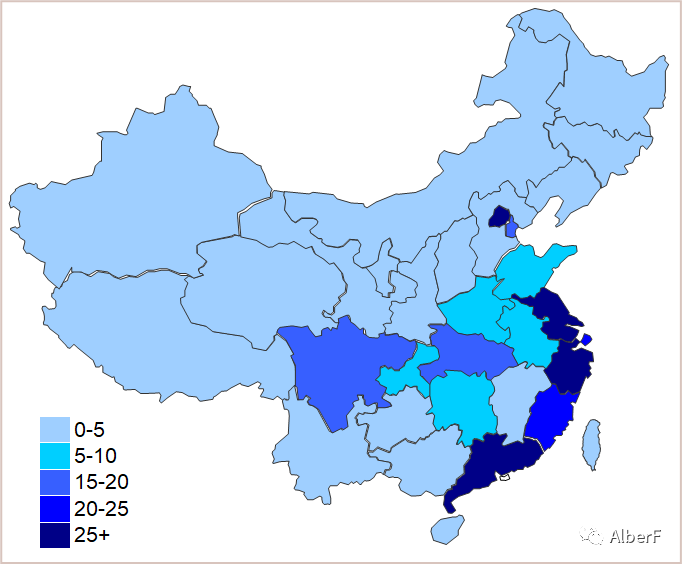
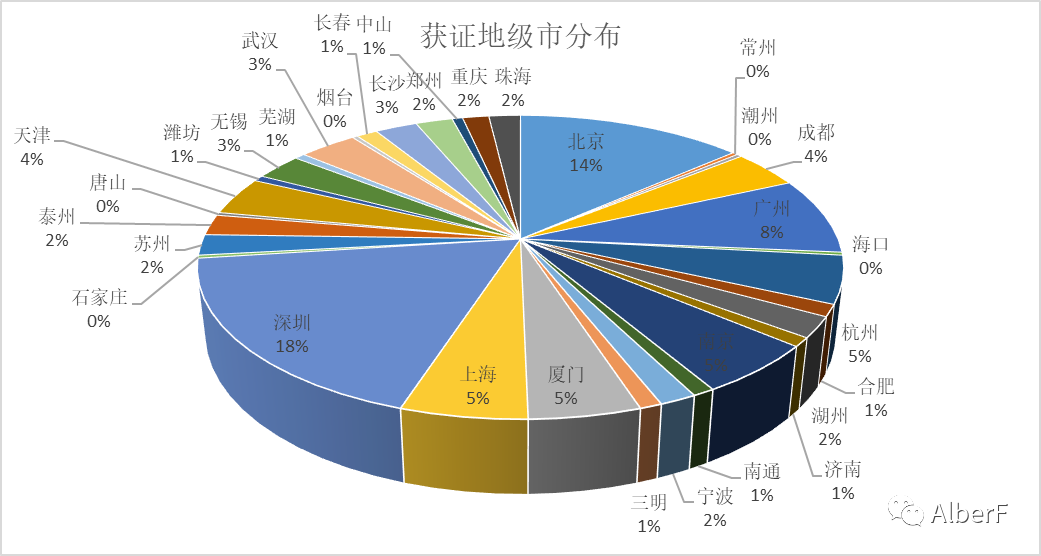
地级市分布
深圳市以57张注册证位居首位
★ 有34个地级市获证,深圳、北京、广州位居前三;PS:IVD从业人员,知道哪里机会多了吗?
★ 各地级市均值为9.64,中位数为6;
方法学统计
化学发光以84张注册证位居第一
★ 经过修正,有23种方法学获证,其中化学发光法、荧光PCR法、胶体金发位居前三;ps:产品命名规则有了,方法学名称是否也规范下
★ 胶化学发光法中36.9%产品在北京和深圳;
★ 胶体金法产品中62%跟新冠相关;
★ 中位数为3,平均值为13.82,分布比较集中;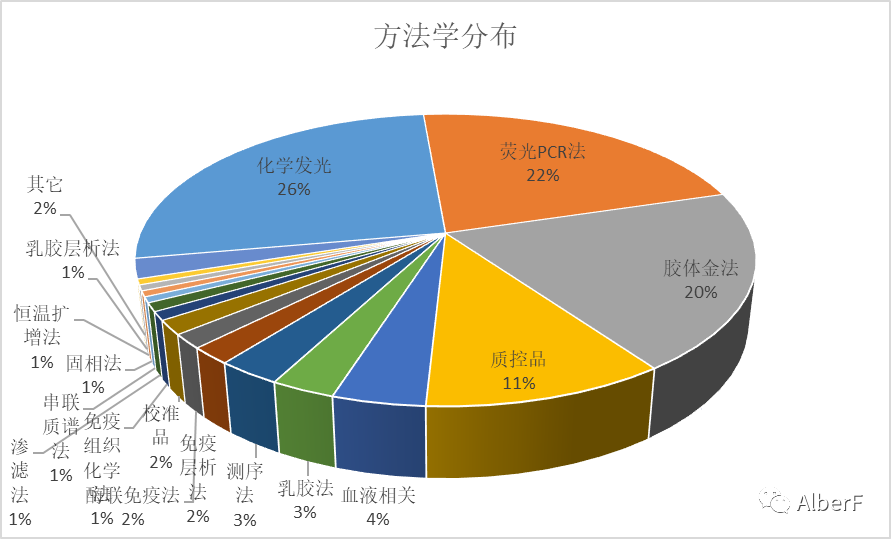
审批时长统计
最长1088天,最短160天(自然日)
★ 共有222个样本,中位数为421天,平均值为475天;
★ 审批时长均值:化学发光法410天(72个样本);荧光PCR法为445天(57个样本);胶体金为434天(25个样本);
★ 现有数据中审批时长最长的是串联质谱法,1035天(2个样本);最短是质控品,240天(18个样本)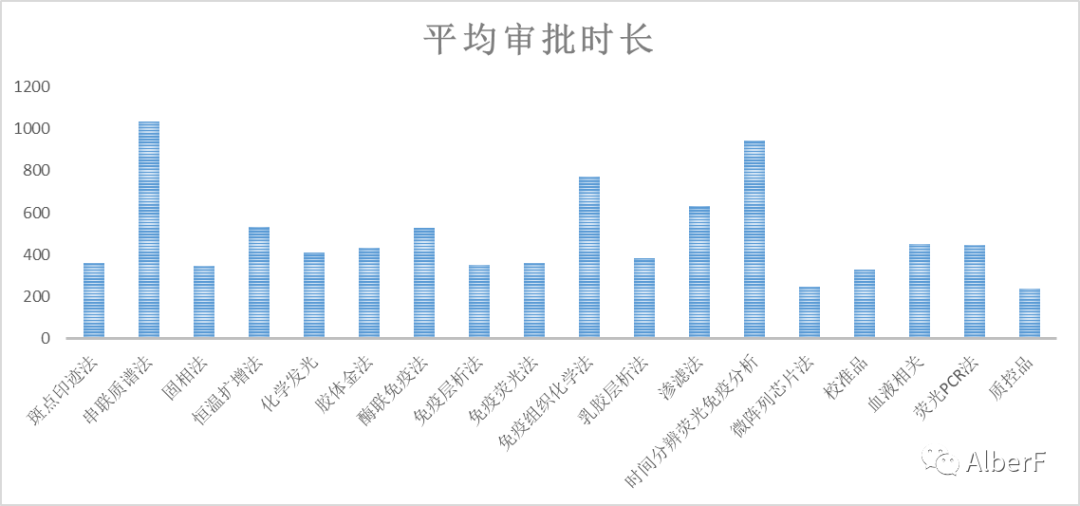


Comments | NOTHING