最近在复习医疗器械临床试验,其中大家比较关注的是——样本量。从网上找到两篇比较好的文献(见后引文),其中一篇还是我们浙江省审评中心的老师发表的。
第1篇文献主要介绍不同的医疗器械临床研究设计,对应的效应指标类型,以及适用的统计分析方法,是一篇综述性的介绍,有助于临床试验大局观的建立;
第2篇文献偏向工具方法,介绍计算样本量所要关注的地方和程序,大致分一下步骤:
- 先区分临床数据的资料性质:一般分为计量资料和计数资料,对应为定量观察和定性观察。对于体外诊断类试剂,一般为计数资料;
- 临床试验的设计类型:优效性设计、非劣效性设计和等效性设计。优效性和非劣效性设计的试验关心的问题是单侧的,对试验组可能优出的程度未加限制。体外诊断试剂一般采用非劣效性设计比较多。对于新试剂,基本采用非劣效性设计?不知理解的对不对。
- 显著性水平α:假设检验中出现I类错误的概率,可理解为出现假阳性错误的概率。一般采用0.05(95%);
- 检验效能β:II类错误的相对应。又称为把握度,在显著性水平取0.05情况下,检验效能取0.2或0.1均可接受。
- 界值δ:即容许误差。这个概念不是很好理解,有待后续或大神指点;
- 总体标准差或总体率:反应数据的变异程度。可以通过预实验得到的样本标准差s或样本率p分别作为总体标准差或总体率的估计值。
- 样本分配:通常采用对照组和试验组等样本量设计。
- 样本脱落问题:不依从或失访等
所需要用到的表1,标准正态百分位数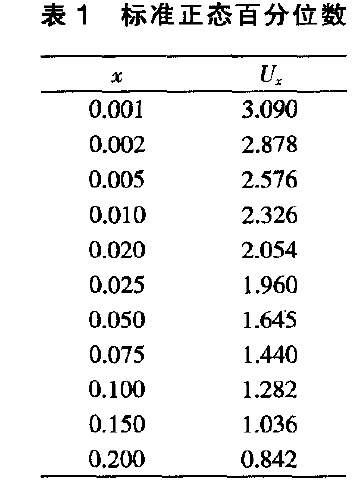
非劣效性设计计数资料的样本量N计算公式:
后面查了一下国家局举办的《统计在诊断产品临床试验中的应用》培训中,李卫老师给出的计算公式跟这篇文献不一致,目前尝未查找来源。(感觉李卫老师的公式,阳性样本量和阴性样本量分开计算,更加简单粗暴,好使)
其中的Za为显著性水平,可从表1中查出
1、《医疗器械临床试验数据的统计分析方法建议》杨笑鹤等 中国医疗器械杂志 临床医学工程 2017年41卷第1期
2、《医疗器械临床试验设计中样本含量的计算》 帅万钧等 医疗卫生装备 2012年7月第33卷 第7期


Comments | NOTHING